
جدول مندلیف
١٤٠٢/١٠/٢٨
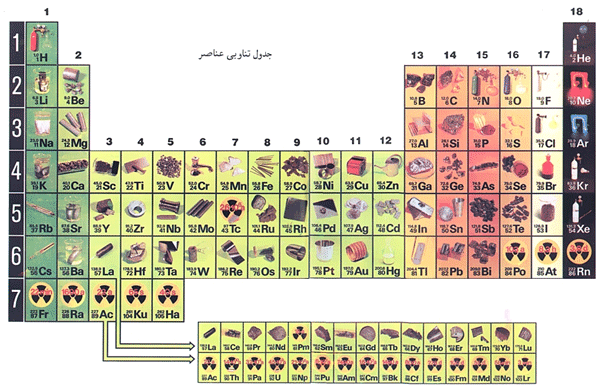
جدل تناوبی عناصر
همه عناصر شیمیایی در جدول تناوبی یا جدول مندلیف در اولویت افزایش اعداد اتمی، در کنار یکدیگر چیده می شوند. خاصیت عناصر در قالب تناوبی یا دوره ای، در این جدول به تکرار می رسد. این عناصر یا به صورت طبیعی یافت می گردد و یا شاید به صورت کاملا مصنوعی در آزمایشگاه ها به تولید برسد. با نگاه به جدول مندلیف با ۱۸ گروه یا ستون و ۷ دوره یا تناوب روبرو خواهید گشت که برخی از آن ها عبارتند از :
- فلزات قلیایی
- فلزات قلیایی خاکی
- هالوژن ها
- گازهای نجیب
- عناصر واسطه
تاریخچه پیدایش جدول مندلیف
تلاش های ابتدایی به جهت گروه بندی عناصر شیمیایی از طریق دانشمندی با نام لاوازیه اتفاق افتاد با این تفاوت که صاحب نقص های متعددی بود. این روند از سوی دانشمند دیگر تکامل یافت و با اصلاحاتی که او بدین ترتیب بندی وارد ساخت تا حدودی نقایصش را برطرف ساخت. همچنان تلاش ها در این مسیر ادامه دار گشت تا اینکه بالاخره استاندارد ترین شیوه طبقه بندی عناصر از سوی استاد شیمی اهل روسیه به نام مندلیف صورت پذیرفت و با بخشیدن نام خود بدان، شهرتش را ثبات بخشید. بعد از گذر زمان و کشف عناصر نوین و ابراز مفهوم عدد اتمی به واسطه دانشمندی به نام موزلی ، جدول مندلیف پستی و بلندی های دیگری را تجربه ساخت اما این مرحله، خط پایان این تغییرات بود و تا به امروز به ثبات خود باقی مانده است.
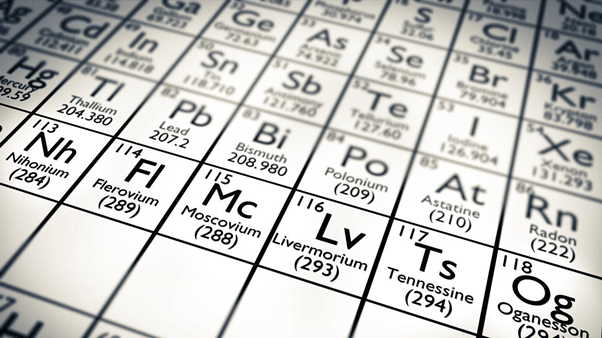
گروه های جدول تناوبی مندلیف
گروه اول
این گروه مجموعه فلزات قلیایی نام دارد که به خانواده لیتیوم نیز شهرت یافته است. این گروه ابتدایی متشکل از عناصر هیدروژن، لیتیوم، سدیم، پتاسیم، روبیدیوم، سزیم و فرانسیوم است.
گروه دوم
گروه بعدی یا فلزات قلیایی خاکی؛ با شهرت خانواده بریلیم شناخته می شوند و عناصر بریلیم، منیزیم، کلسیم، استرانسیم، باریم و رادیم را تحت پوشش خود قرار می دهند.
گروه ۳ تا ۱۲
فلزات در گروه ۳ تا ۱۲ جای داده شده اند. زیر لایه d این عناصر به شکل کاملا جزئی در حال هموار گشتن است. گروه ۳ وسیع تر از آن می باشد که به صورت کامل در ستون سوم جای داده شود. از همین رو عناصر ۵۷ تا ۷۱ جدول تناوبی، دسته ای از لانتانید ها تخت پوشش قرار می دهند. مضاعف بر آن عنصر های شماره ۸۹ تا ۱۰۳، متشکل از گروهی با نام اکتینید ها هستند. این مورد را از یاد نبرید که اکتینیدها، رادیواکتیو هستند. لانتانیدها و اکتینیدها به نام فلزات واسطه داخلی قابل شناخت هستند.
گروه ۱۳
خانواده بور در گروه ۱۳ قرار می گیرند و عناصر آن عبارتند از:
- عناصر بور
- آلومینیوم
- گالیم
- اینیدیم
- تالیم و …
گروه ۱۴
عنصر های چون کربن، سیلیسیم، ژرمانیم، قلع و سرب و … در گروه شماره ۱۴ به ترتیب چیده می شوند و شهرت خانواده کربن را از آن خود می سازند.
گروه ۱۵
خانواده نیتروژن یا همان گروه شماره ۱۵ جدول مندلیف با زیر مجموعه ای از عناصر غیر فلزی به قرار زیر معرفی می گردد :
- نیتروژن
- فسفر
- آرسنیک
- آنتیموان
- بیسموت و …
گروه ۱۶
خانواده اکسیژن یا گروه شماره ۱۶ در جدول مندلیف به معرفی ویژگی های عناصر نافلزی اکسیژن، گوگرد، سلنیم، تلوریم، پلونیم و … می پردازد.
گروه ۱۷
هالوژن ها نام گروه شماره ۱۷ است و معرف عناصر غیر فلزی فلوئور، کلر، برم، ید، استاتین و … هستند.
گروه ۱۸
گازهای نجیب یا بدور از کمترین اثری در گروه ۱۸ قرار می گیرند و برای آشناییت با آن ها می توان به عناصر هلیوم، نئون، آرگون، کریپتون، زنون، رادون و … اشاره داشت.
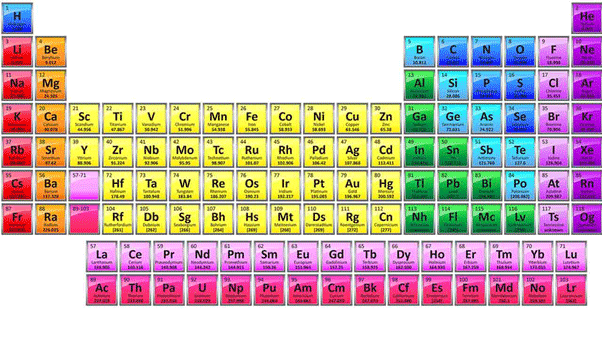
چرا از جدول تناوبی یا مندلیف استفاده می گردد؟
جدول تناوبی و یا مندلیف مهمترین مرجع در تحقیقات و برسی های گروه های شیمیدان، فیزیکدان یا مهندسین بشمار می آیند. کسب اطلاعات به جهت مطالعه و مراجعه جدول تناوبی به قرار زیر است :
- عدد اتمی عناصر
- اطلاع از نام تمامی عناصر ها و نماد های مرتبط به آن
- وزن اتمی عنصر ها
- پیکربندی الکترونی عنصر ها
آزمایش شیمی
برای خرید مواد شیمیایی گرید آزمایشگاهی با همکاران ما تماس حاصل فرمایید.
استفاده از مقالات سایت با ذکر منبع بلامانع است
